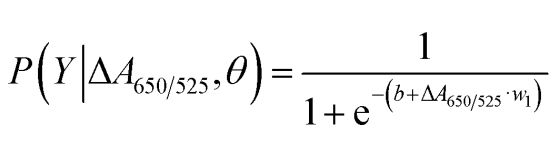Ранняе выяўленне раку на аснове вадкаснай біяпсіі — гэта новы кірунак выяўлення і дыягностыкі раку, прапанаваны Нацыянальным інстытутам раку ЗША ў апошнія гады з мэтай выяўлення ранняга раку або нават перадракавых паражэнняў. Ён шырока выкарыстоўваецца ў якасці новага біямаркера для ранняй дыягностыкі розных злаякасных новаўтварэнняў, у тым ліку раку лёгкіх, пухлін страўнікава-кішачнага гасцінца, гліём і гінекалагічных пухлін.
З'яўленне платформаў для ідэнтыфікацыі біямаркераў метыляцыйнага ландшафту (Methylscape) мае патэнцыял значна палепшыць існуючы ранні скрынінг раку, дазваляючы пацыентам знаходзіцца на самых ранніх стадыях лячэння.
Нядаўна даследчыкі распрацавалі простую і прамую платформу для выяўлення ландшафту метылявання на аснове залатых наначасціц, дэкараваных цыстэамінам (Cyst/AuNPs), у спалучэнні з біясенсарам на базе смартфона, што дазваляе хутка праводзіць ранні скрынінг шырокага спектру пухлін. Ранні скрынінг на лейкемію можа быць праведзены на працягу 15 хвілін пасля экстракцыі ДНК з узору крыві з дакладнасцю 90,0%. Назва артыкула: Хуткае выяўленне ракавай ДНК у крыві чалавека з выкарыстаннем AuNPs, пакрытых цыстэамінам, і смартфона з падтрымкай машыннага навучання.
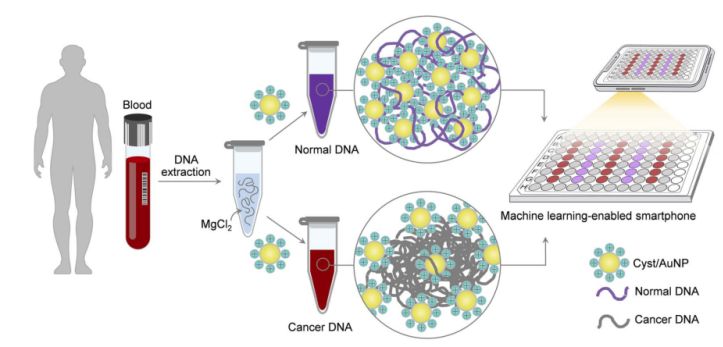
Малюнак 1. Простая і хуткая платформа для выяўлення раку з дапамогай кампанентаў Cyst/AuNPs можа быць створана ў два простыя крокі.
Гэта паказана на малюнку 1. Спачатку для растварэння фрагментаў ДНК выкарыстоўвалі водны раствор. Затым да змешанага раствора дадавалі цысты/наначасціцы з асновай (AuNPs). Нармальная і злаякасная ДНК маюць розныя ўласцівасці метылявання, у выніку чаго ўтвараюцца фрагменты ДНК з рознымі мадэлямі самазборкі. Нармальная ДНК агрэгуе свабодна і ў рэшце рэшт агрэгуе цысты/наначасціцы з асновай, што прыводзіць да зрушэння колеру цысты/наначасціц у чырвоны колер, так што змяненне колеру з чырвонага на фіялетавы можна назіраць няўзброеным вокам. Наадварот, унікальны профіль метылявання ракавай ДНК прыводзіць да ўтварэння больш буйных кластараў фрагментаў ДНК.
Здымкі 96-лункавых планшэтаў былі зроблены з дапамогай камеры смартфона. ДНК рака вымяралася смартфонам, абсталяваным машынным навучаннем, у параўнанні з метадамі, заснаванымі на спектраскапіі.
Скрынінг раку ў рэальных пробах крыві
Каб пашырыць магчымасці выкарыстання сэнсарнай платформы, даследчыкі ўжылі датчык, які паспяхова адрозніваў нармальную і ракавую ДНК у рэальных узорах крыві. Патэрны метылявання ў сайтах CpG эпігенетычна рэгулююць экспрэсію генаў. Амаль ва ўсіх тыпах раку назіралася чаргаванне змен у метыляванні ДНК і, такім чынам, у экспрэсіі генаў, якія спрыяюць тумарыгенезу.
У якасці мадэлі для іншых відаў раку, звязаных з метыляваннем ДНК, даследчыкі выкарысталі ўзоры крыві пацыентаў з лейкеміяй і здаровых людзей кантрольнай групы, каб даследаваць эфектыўнасць ландшафту метылявання ў дыферэнцыяцыі лейкемічных відаў раку. Гэты біямаркер ландшафту метылявання не толькі пераўзыходзіць існуючыя метады хуткага скрынінга на лейкемію, але і дэманструе магчымасць пашырэння гэтага простага і зразумелага аналізу на ранняе выяўленне шырокага спектру відаў раку.
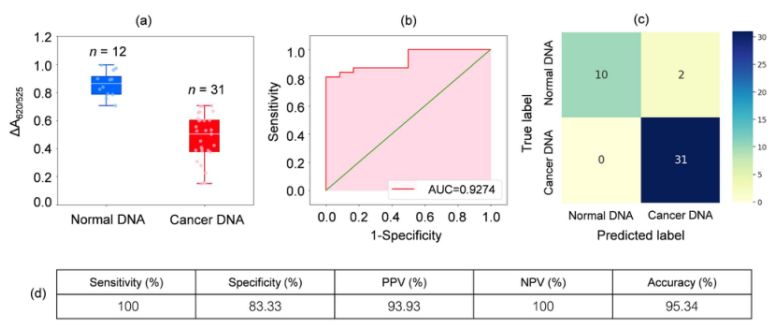
Была прааналізавана ДНК з узораў крыві 31 пацыента з лейкеміяй і 12 здаровых асоб. Як паказана на дыяграме на малюнку 2a, адноснае паглынанне ўзораў раку (ΔA650/525) было ніжэйшым, чым у ДНК з нармальных узораў. Гэта было ў асноўным звязана з павышанай гідрафобнасцю, якая прывяла да шчыльнай агрэгацыі ракавай ДНК, што перашкаджала агрэгацыі Cyst/AuNPs. У выніку гэтыя наначасціцы былі цалкам дыспергаваныя ў вонкавых пластах ракавых агрэгатаў, што прывяло да рознай дысперсіі Cyst/AuNPs, адсарбаваных на нармальнай і ракавай ДНК. Затым ROC-крывыя былі створаны шляхам змены парога ад мінімальнага значэння ΔA650/525 да максімальнага значэння.
Малюнак 2.(a) Адносныя значэнні паглынання раствораў цыст/AuNPs, якія паказваюць наяўнасць нармальнай (сіні) і ракавай (чырвоны) ДНК у аптымізаваных умовах.
(DA650/525) скрынкавых дыяграм; (b) ROC-аналіз і ацэнка дыягнастычных тэстаў. (c) Матрыца блытаніны для дыягностыкі здаровых і анкалагічных пацыентаў. (d) Адчувальнасць, спецыфічнасць, станоўчая прагнастычная каштоўнасць (ППЗ), адмоўная прагнастычная каштоўнасць (АДЗ) і дакладнасць распрацаванага метаду.
Як паказана на малюнку 2b, плошча пад крывой ROC (AUC = 0,9274), атрыманая для распрацаванага датчыка, прадэманстравала высокую адчувальнасць і спецыфічнасць. Як відаць з скрынкавай дыяграмы, самая нізкая кропка, якая прадстаўляе нармальную групу ДНК, дрэнна аддзелена ад самай высокай кропкі, якая прадстаўляе групу ракавай ДНК; таму для адрознення нармальных і ракавых груп была выкарыстана лагістычная рэгрэсія. Улічваючы набор незалежных зменных, яна ацэньвае верагоднасць узнікнення падзеі, напрыклад, ракавай або нармальнай групы. Залежная зменная мае значэнні ад 0 да 1. Такім чынам, вынік з'яўляецца верагоднасцю. Мы вызначылі верагоднасць выяўлення раку (P) на аснове ΔA650/525 наступным чынам.
дзе b=5,3533, w1=-6,965. Для класіфікацыі ўзораў верагоднасць менш за 0,5 паказвае на нармальны ўзор, а верагоднасць 0,5 або вышэй — на ракавы ўзор. На малюнку 2c паказана матрыца блытаніны, атрыманая ў выніку перакрыжаванай праверкі без уліку фактару, якая выкарыстоўвалася для праверкі стабільнасці метаду класіфікацыі. На малюнку 2d падсумавана ацэнка дыягнастычнага тэсту метаду, уключаючы адчувальнасць, спецыфічнасць, станоўчую прагнастычную каштоўнасць (ППЗ) і адмоўную прагнастычную каштоўнасць (АПРЗ).
Біясенсары на базе смартфонаў
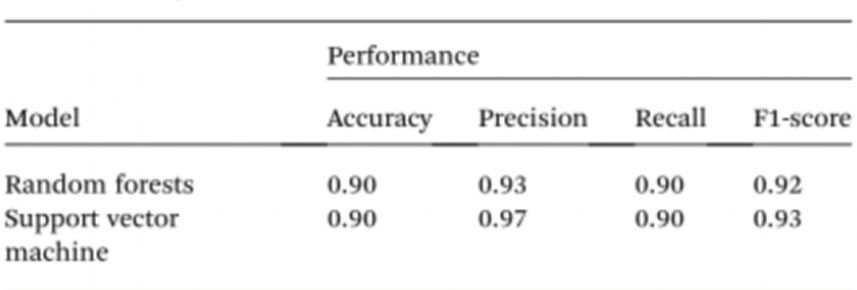
Каб яшчэ больш спрасціць тэставанне ўзораў без выкарыстання спектрафатометраў, даследчыкі выкарысталі штучны інтэлект (ШІ) для інтэрпрэтацыі колеру раствора і адрознення нармальных і ракавых асобін. Улічваючы гэта, камп'ютэрны зрок быў выкарыстаны для перакладу колеру раствора Cyst/AuNPs у нармальную ДНК (фіялетавы) або ракавую ДНК (чырвоны) з выкарыстаннем малюнкаў 96-лункавых пласцін, зробленых з дапамогай камеры мабільнага тэлефона. Штучны інтэлект можа знізіць выдаткі і палепшыць даступнасць інтэрпрэтацыі колеру раствораў наначасціц без выкарыстання якіх-небудзь аптычных аксесуараў для смартфонаў. Нарэшце, дзве мадэлі машыннага навучання, у тым ліку Random Forest (RF) і Support Vector Machine (SVM), былі навучаны для пабудовы мадэляў. Абедзве мадэлі RF і SVM правільна класіфікавалі ўзоры як станоўчыя і адмоўныя з дакладнасцю 90,0%. Гэта сведчыць аб тым, што выкарыстанне штучнага інтэлекту ў біясенсарынгу на аснове мабільных тэлефонаў цалкам магчыма.
Малюнак 3. (a) Мэтавы клас раствора, запісаны падчас падрыхтоўкі ўзору для этапу атрымання выявы. (b) Прыклад выявы, зробленай падчас этапу атрымання выявы. (c) Інтэнсіўнасць колеру раствора цысты/AuNPs у кожнай лунцы 96-лункавага планшэта, вынятага з выявы (b).
Выкарыстоўваючы Cyst/AuNP, даследчыкі паспяхова распрацавалі простую сэнсарную платформу для выяўлення ландшафту метылявання і датчык, здольны адрозніваць нармальную ДНК ад ракавай ДНК пры выкарыстанні рэальных узораў крыві для скрынінга лейкеміі. Распрацаваны датчык прадэманстраваў, што ДНК, вынятая з рэальных узораў крыві, здольная хутка і эканамічна эфектыўна выяўляць невялікую колькасць ракавай ДНК (3 нМ) у пацыентаў з лейкеміяй за 15 хвілін і паказала дакладнасць 95,3%. Для далейшага спрашчэння тэсціравання ўзораў, ліквідуючы неабходнасць у спектрафатометры, было выкарыстана машыннае навучанне для інтэрпрэтацыі колеру раствора і адрознення нармальных і ракавых асоб з дапамогай фатаграфіі мабільнага тэлефона, і дакладнасць таксама была дасягнута на ўзроўні 90,0%.
Спасылка: DOI: 10.1039/d2ra05725e
Час публікацыі: 18 лютага 2023 г.
 中文网站
中文网站