Nat Med | Мультыомічны падыход да картаграфавання інтэграванага пухліннага, імуннага і мікробнага ландшафту каларэктальнага раку раскрывае ўзаемадзеянне мікрабіёма з імуннай сістэмай
Нягледзячы на тое, што ў апошнія гады біямаркеры першаснага рака тоўстай кішкі былі шырока вывучаны, сучасныя клінічныя рэкамендацыі абапіраюцца толькі на стадыю пухліны-лімфатычных вузлоў-метастазаў і выяўленне дэфектаў рэпарацыі няспраўнасцей ДНК (MMR) або мікрасатэлітнай нестабільнасці (MSI) (у дадатак да стандартнага паталагічнага тэставання) для вызначэння рэкамендацый па лячэнні. Даследчыкі адзначылі адсутнасць сувязі паміж імуннымі рэакцыямі на аснове экспрэсіі генаў, мікробнымі профілямі і пухліннай стромой у кагорце каларэктальных ракаў Атласа геному рака (TCGA) і выжывальнасцю пацыентаў.
Па меры развіцця даследаванняў паведамлялася, што колькасныя характарыстыкі першаснага каларэктнага раку, у тым ліку клеткавая, імунная, страмальная або мікробная прырода раку, значна карэлююць з клінічнымі вынікамі, але разуменне таго, як іх узаемадзеянне ўплывае на вынікі лячэння пацыентаў, усё яшчэ абмежаванае.
Каб высветліць сувязь паміж фенатыпічнай складанасцю і вынікам, каманда даследчыкаў з Інстытута медыцынскіх даследаванняў Сідра ў Катары нядаўна распрацавала і пацвердзіла інтэграваную шкалу (mICRoScore), якая вызначае групу пацыентаў з добрымі паказчыкамі выжывальнасці шляхам спалучэння характарыстык мікрабіёма і канстант імуннага адрыньвання (ICR). Каманда правяла комплексны геномны аналіз свежазамарожаных узораў ад 348 пацыентаў з першасным каларэктальным ракам, уключаючы секвенаванне РНК пухлін і супастаўнай здаровай каларэктальнай тканкі, секвенаванне ўсяго экзома, глыбокае секвенаванне генаў Т-клетачных рэцэптараў і 16S бактэрыяльнай рРНК, дапоўненае секвенаваннем усяго геному пухліны для далейшай характарыстыкі мікрабіёма. Даследаванне было апублікавана ў часопісе Nature Medicine пад назвай «Інтэграваны атлас пухлін, імунітэту і мікрабіёма рака тоўстай кішкі».

Артыкул апублікаваны ў часопісе Nature Medicine
Агляд AC-ICAM
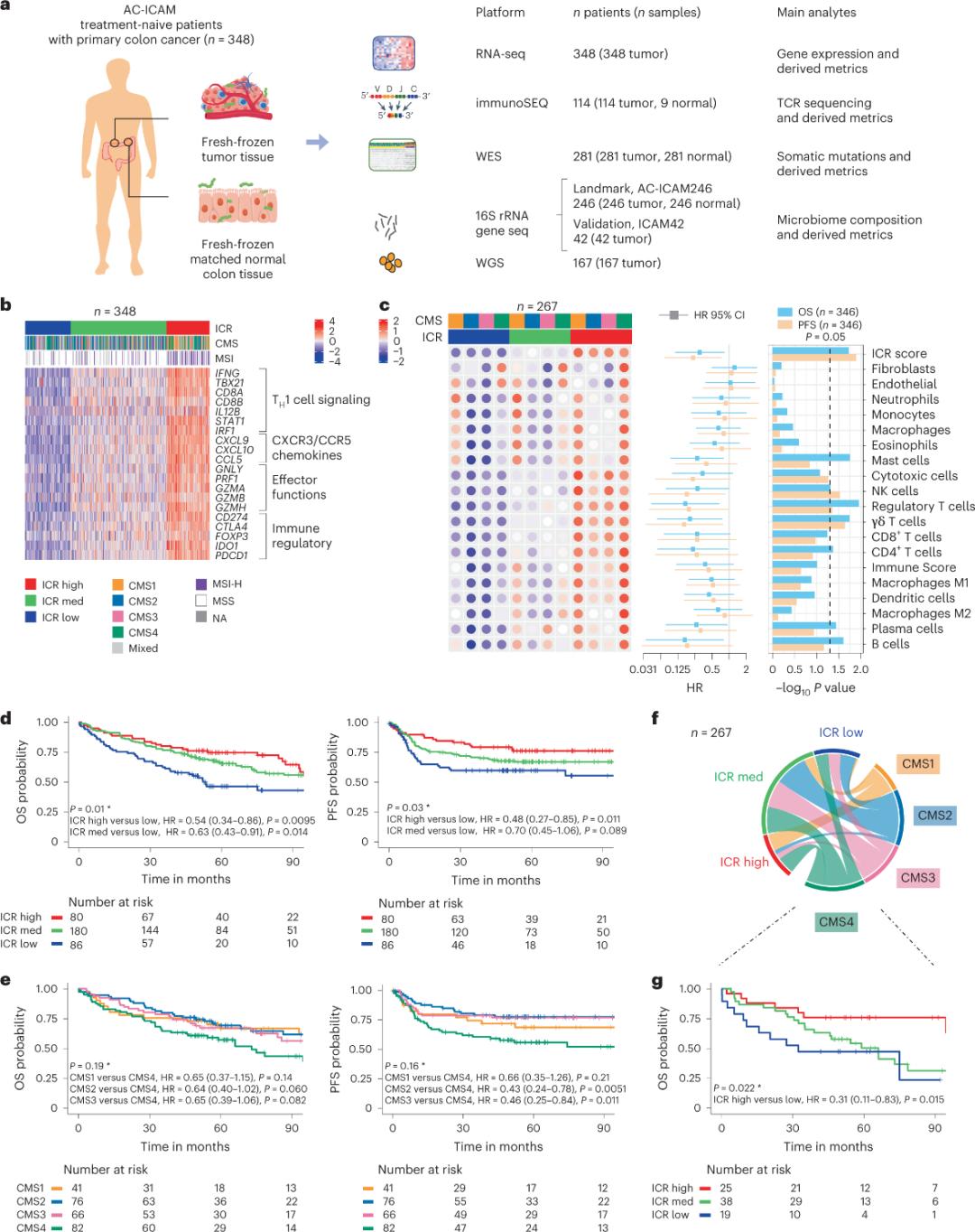
Даследчыкі выкарысталі артаганальную геномную платформу для аналізу свежазамарожаных узораў пухлін і супастаўнай прылеглай здаровай тканіны тоўстай кішкі (пары пухліна-нармальная тканіна) ад пацыентаў з гісталагічным дыягназам рака тоўстай кішкі без сістэмнай тэрапіі. На падставе поўнаэкзомнага секвенавання (WES), кантролю якасці дадзеных РНК-секвенавання і скрынінга крытэрыяў уключэння былі захаваны геномныя дадзеныя 348 пацыентаў і выкарыстаны для далейшага аналізу з сярэднім перыядам назірання 4,6 года. Даследчая група назвала гэты рэсурс Sidra-LUMC AC-ICAM: Карта і кіраўніцтва па ўзаемадзеянні імуннай сістэмы, рака і мікрабіёма (малюнак 1).
Малекулярная класіфікацыя з выкарыстаннем ICR
Атрымаўшы модульны набор імунных генетычных маркераў для бесперапыннага імунакантролю раку, які называецца імуннай канстантай адрыньвання (ICR), даследчая група аптымізавала ICR, аб'яднаўшы яго ў 20-генную панэль, якая ахоплівае розныя тыпы раку, у тым ліку меланому, рак мачавой бурбалкі і рак малочнай залозы. ICR таксама асацыюецца з імунатэрапеўтычным адказам пры розных тыпах раку, у тым ліку раку малочнай залозы.
Спачатку даследчыкі пацвердзілі ICR-сігнатуру кагорты AC-ICAM, выкарыстоўваючы падыход сумеснай класіфікацыі на аснове генаў ICR, каб класіфікаваць кагорту на тры кластары/імунныя падтыпы: высокі ICR (гарачыя пухліны), сярэдні ICR і нізкі ICR (халодныя пухліны) (Малюнак 1b). Даследчыкі ахарактарызавалі імунную схільнасць, звязаную з кансенсуснымі малекулярнымі падтыпамі (CMS), класіфікацыяй раку тоўстай кішкі на аснове транскрыптомаў. Катэгорыі CMS уключалі CMS1/імунны, CMS2/кананічны, CMS3/метабалічны і CMS4/мезенхімальны. Аналіз паказаў, што паказчыкі ICR адмоўна карэлявалі з пэўнымі шляхамі ракавых клетак ва ўсіх падтыпах CMS, а станоўчая карэляцыя з імунасупрэсіўнымі і звязанымі са стромай шляхамі назіралася толькі ў пухлінах CMS4.
Ва ўсіх КМС колькасць падгруп натуральных кілерных (NK) і Т-клетак была найвышэйшай у падтыпах ICR з высокім імунітэтам, з большай зменлівасцю ў іншых падгрупах лейкацытаў (малюнак 1c). Імунныя падтыпы ICR мелі розную выжывальнасць і выжывальнасць без прагрэсавання, з прагрэсіўным павелічэннем ICR ад нізкага да высокага (малюнак 1d), што пацвярджае прагнастычную ролю ICR пры каларэктальным раку.
Малюнак 1. Дызайн даследавання AC-ICAM, імуназалежная генная сігнатура, імунныя і малекулярныя падтыпы і выжывальнасць.
ICR фіксуе ўзбагачаныя пухлінай, клональна ампліфікаваныя Т-клеткі
Паведамлялася, што толькі невялікая частка Т-клетак, якія інфільтруюць пухлінную тканіну, спецыфічныя для пухлінных антыгенаў (менш за 10%). Такім чынам, большасць унутрыпухлінных Т-клетак называюцца сведкамі Т-клетак (сведкі Т-клетак). Найбольш моцная карэляцыя з колькасцю звычайных Т-клетак з прадуктыўнымі Т-клетачнымі рэпрэзентацыямі (Т-клеткі-папярэднікі) назіралася ў субпапуляцыях стромальных клетак і лейкацытаў (выяўленых з дапамогай РНК-секвенавання), што можна выкарыстоўваць для ацэнкі субпапуляцый Т-клетак (малюнак 2a). У кластарах ICR (агульная і класіфікацыя CMS) найвышэйшая кланальнасць імунных SEQ TCR назіралася ў групах ICR-high і CMS падтыпу CMS1/імунітэт (малюнак 2c), з найвышэйшай доляй пухлін з высокім ICR. Выкарыстоўваючы ўвесь транскрыптом (18 270 генаў), шэсць генаў ICR (IFNG, STAT1, IRF1, CCL5, GZMA і CXCL10) былі сярод дзесяці генаў, станоўча звязаных з кланальнасцю імунных SEQ TCR (малюнак 2d). Кланальнасць TCR па дадзеных ImmunoSEQ мацней карэлявала з большасцю генаў ICR, чым карэляцыі, якія назіраліся з выкарыстаннем маркераў CD8+, якія рэагуюць на пухліну (малюнак 2f і 2g). У заключэнне, вышэйзгаданы аналіз сведчыць аб тым, што сігнатура ICR фіксуе прысутнасць узбагачаных пухлінай, клональна ампліфікаваных Т-клетак і можа растлумачыць яе прагнастычныя наступствы.
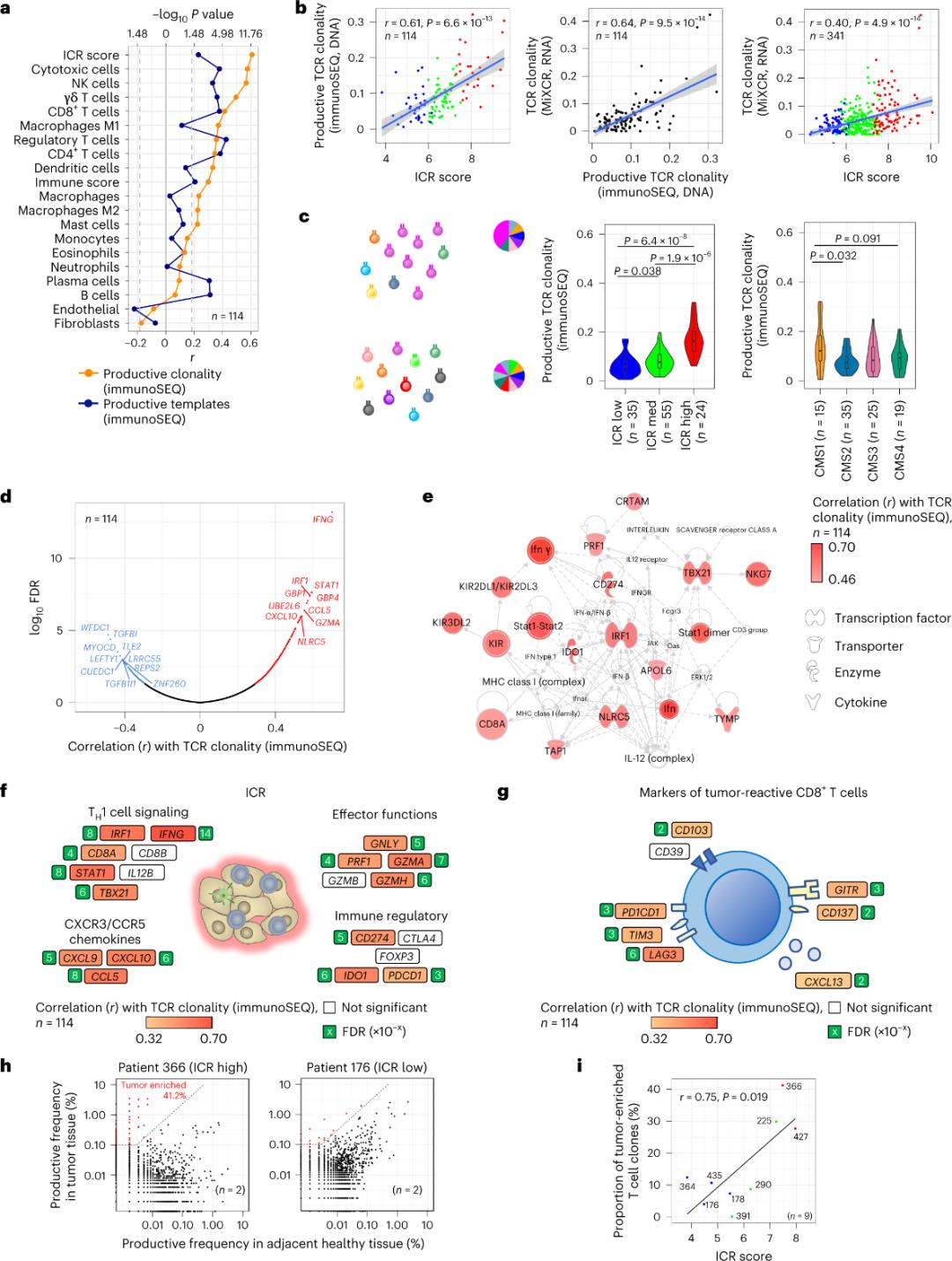
Малюнак 2. Паказчыкі TCR і карэляцыя з імуналагічнымі генамі, імуннымі і малекулярнымі падтыпамі.
Склад мікрабіёма ў здаровых тканінах і тканінах тоўстай кішкі, якія хварэюць на рак
Даследчыкі правялі секвенаванне 16S рРНК з выкарыстаннем ДНК, вынятай з супадаючай пухліны і здаровай тканіны тоўстай кішкі ад 246 пацыентаў (малюнак 3a). Для праверкі даследчыкі дадаткова прааналізавалі дадзеныя секвенавання генаў 16S рРНК з дадатковых 42 узораў пухлін, у якіх не было супадаючай нармальнай ДНК, даступнай для аналізу. Спачатку даследчыкі параўналі адносную колькасць флоры паміж супадаючымі пухлінамі і здаровай тканінай тоўстай кішкі. Колькасць Clostridium perfringens была значна павялічана ў пухлінах у параўнанні са здаровымі ўзорамі (малюнкі 3a-3d). Не было выяўлена істотнай розніцы ў альфа-разнастайнасці (разнастайнасць і колькасць відаў у адным узоры) паміж пухлінамі і здаровымі ўзорамі, і назіралася невялікае зніжэнне мікробнай разнастайнасці ў пухлінах з высокім ICR у параўнанні з пухлінамі з нізкім ICR.
Каб выявіць клінічна значныя сувязі паміж мікробнымі профілямі і клінічнымі вынікамі, даследчыкі імкнуліся выкарыстаць дадзеныя секвенавання генаў 16S рРНК для вызначэння асаблівасцей мікрабіёма, якія прадказваюць выжывальнасць. У AC-ICAM246 даследчыкі правялі рэгрэсійную мадэль OS Cox, у якой былі адабраны 41 прыкмета з ненулявымі каэфіцыентамі (звязанымі з дыферэнцыяльнай рызыкай смяротнасці), якія называюцца класіфікатарамі MBR (малюнак 3f).
У гэтай навучальнай кагорце (ICAM246) нізкі бал MBR (MBR < 0, нізкі MBR) быў звязаны са значна меншай рызыкай смерці (85%). Даследчыкі пацвердзілі сувязь паміж нізкім MBR (рызыкай) і працяглай агульнай выжывальнасцю ў дзвюх незалежна правераных кагортах (ICAM42 і TCGA-COAD). (Малюнак 3) Даследаванне паказала моцную карэляцыю паміж эндагастральнымі кокамі і баламі MBR, якія былі падобнымі ў пухліне і здаровай тканіны тоўстай кішкі.
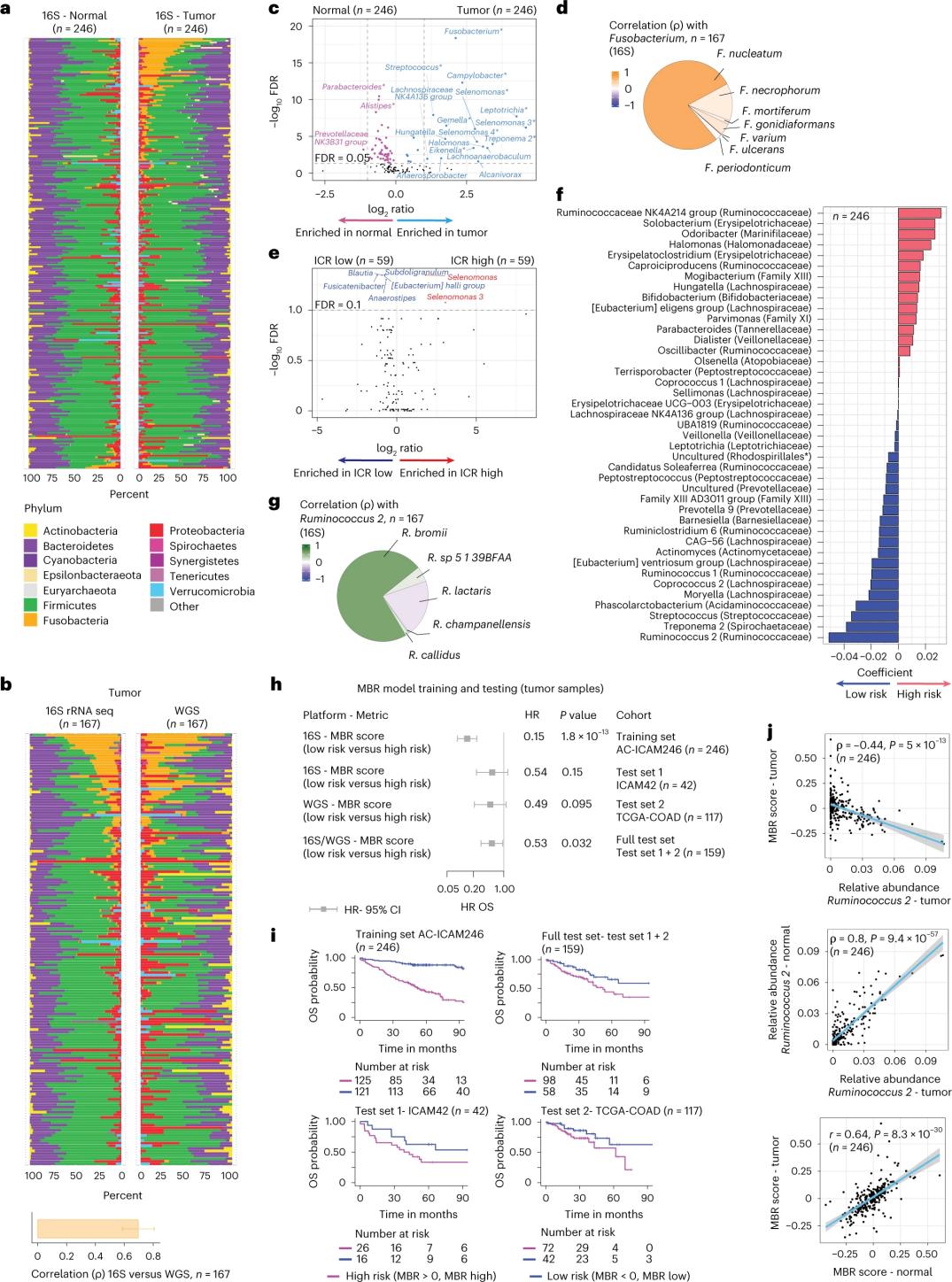
Малюнак 3. Мікрабіём у пухліне і здаровых тканінах і сувязь з ICR і выжывальнасцю пацыентаў.
Выснова
Мультымічны падыход, які выкарыстоўваецца ў гэтым даследаванні, дазваляе дэталёва выявіць і прааналізаваць малекулярную сігнатуру імуннага адказу пры каларэктальным раку і раскрывае ўзаемадзеянне паміж мікрабіёмам і імуннай сістэмай. Глыбокае секвенаванне Т-клетак пухліны і здаровых тканін паказала, што прагнастычны эфект ІЦР можа быць абумоўлены яго здольнасцю захопліваць узбагачаныя пухлінай і, магчыма, спецыфічныя для пухліннага антыгена Т-клетачныя клоны.
Аналізуючы склад мікрабіёма пухліны з выкарыстаннем секвенавання гена 16S рРНК ва ўзорах AC-ICAM, каманда вызначыла мікрабіёмную сігнатуру (бал рызыкі MBR) з высокай прагнастычнай каштоўнасцю. Нягледзячы на тое, што гэтая сігнатура была атрымана з узораў пухліны, існавала моцная карэляцыя паміж здаровай кішкай і балам рызыкі MBR пухліны, што сведчыць аб тым, што гэтая сігнатура можа адлюстроўваць склад мікрабіёма кішачніка пацыентаў. Аб'яднаўшы балы ICR і MBR, стала магчымым вызначыць і пацвердзіць мультыомны біямаркер студэнтаў, які прагназуе выжывальнасць пацыентаў з ракам тоўстай кішкі. Мультыомны набор даных даследавання дае рэсурс для лепшага разумення біялогіі рака тоўстай кішкі і дапамагае ў распрацоўцы персаналізаваных тэрапеўтычных падыходаў.
Час публікацыі: 15 чэрвеня 2023 г.
 中文网站
中文网站